Lancet. 2022;399(10335):1646-1663.
【ポイント】
-
糸球体腎炎の根本的な原因や発症機序の解明が進み、糸球体腎炎の分類は、生検パターンに基づくアプローチよりも疾患の原因に基づくアプローチが行われることが多くなった
-
治療法は進歩し続けており、病態生理の理解・その原因を理解することが重要
【急性糸球体腎炎総論】
糸球体腎炎の原因は様々で、臨床経過も様々
そのうちfull-blown nephritic syndrome・急速進行性糸球体腎炎(Rapidly progressive glomerulonephritis: RPGN)は、まれな部類に入る
表:糸球体疾患に特徴的な臨床所見
◎診断
①初期評価
-
腎生検の前に血液・尿検査を行う
-
腎生検を行わなくても診断が確定することはよくある
-
◎検査項目は以下の通り
②腎生検
-
診断のゴールドスタンダードは腎生検
-
疾患原因・急性度・重症度の理解に役立つ
-
原因に基づいて糸球体腎炎を分類する
-

表:糸球体腎炎の分類・概要
③一般的な糸球体腎炎の管理
-
減塩、RAS阻害薬による血圧管理(目標収縮期血圧<120mmHg)
-
食事療法…蛋白制限に関しては蛋白尿の程度・腎機能によって決定する
-
生活指導…禁煙、体重減少、定期的な身体活動など→心血管リスクを下げる
-
腎機能悪化時の腎代替療法準備
【急性糸球体腎炎各論】
①感染関連糸球体腎炎
感染後糸球体腎炎(PIGN)と活動性感染関連糸球体腎炎の2つに分かれる
◎臨床所見
-
感染後糸球体腎炎(PIGN)
-
感染エピソード解決後の1-6週間後の発症が多い
-
多くは小児期発症だが成人にも発症し、60歳以降で多い
-
大半は無症状
-
小児は腎生検不要のことが多いが、成人・C3低値遷延(3ヵ月以上)の場合は腎生検推奨
-
活動性感染関連糸球体腎炎
-
起因菌…ブドウ球菌(staphylococcus-associated glomerulonephritis: SAGN)、レンサ球菌、Streptococcus mutans、HACEK(Haemophilus spp, Aggregatibacter spp, Cardiobacterium hominis, Eikenella corrodens, Kingella spp)など
-
SAGNは糖尿病のある高齢男性、静注薬物乱用の若年者で多い
-
-
感染症罹患中の発症が特徴的
-
30-50%でC3低値、50%で血液培養陽性
-
毛細血管壁に沿った免疫複合体の沈着と二次的な補体の活性化から起こるとされる
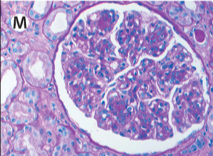
◎病理
-
光学顕微鏡…毛細血管内の細胞過形成、好中球等の白血球浸潤を伴うびまん性増殖性傷害パターン
-
免疫蛍光染色
-
PIGN…C3陽性、IgGの程度は低い。染色パターンは毛細血管壁に沿った顆粒状I(garland pattern)・散在してランダムに分布する細かい粒状の沈着(starry sky pattern)など。
-
SAGN…IgA陽性が多く、IgG陽性も見られうる。メサンギウム・毛細血管壁辺縁のC3陽性の場合もあり、原発性IgA腎症に類似している
-
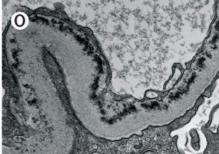
電子顕微鏡…上皮下のコブ状dense depositが典型的(PIGN>SAGN)
◎治療
-
基本的には支持療法…高血圧・体液貯留・浮腫のコントロール
-
感染症がactiveの場合、抗生剤
-
免疫抑制薬の役割は不明
-
併存疾患のある高齢者の場合、致死的な場合がある
-
予後
-
小児は予後良好…血清Creは4週間以内に改善し、血尿も3−6ヶ月で改善する
-
成人は症状継続する場合が多い。糖尿病患者の場合予後不良。
②IgA腎症
糸球体腎症の原因として最多。東アジアで有病率が高い。
二次性原因に肝疾患、セリアック病、強直性脊推炎等がある
◎臨床所見
-
IgA腎症患者の<10%にネフローゼ症候群が見られる
-
急性腎不全…<5%で発生
-
鋳型赤血球による可逆性急性尿細管障害→肉眼的血尿に続発 or 急速進行性糸球体腎炎
-
他の糸球体腎炎よりも予後が悪いことが知られている
-
予後予測…国際IgA腎症ネットワークからのリスク予測ツールが有用(JAMA Intern Med, 179 (2019), pp. 942-952)
-
全身型IgA腎症は、IgA血管炎と呼ばれる
-
小児に多く、小児では予後良好、成人では予後色々。
-
症状…白血球破砕性血管炎(腰より下で顕著)、関節痛、腹痛、腎臓病変など
◎病理
-
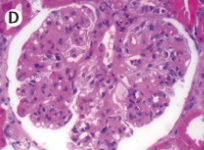
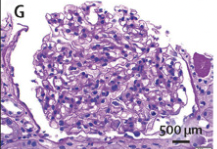
光学顕微鏡…メサンギウム増殖性糸球体腎炎が典型的
-
メサンギウム増殖性糸球体腎炎
-
-
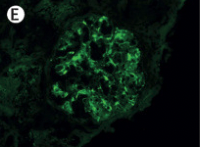
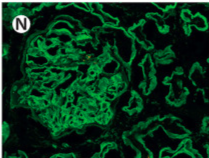
免疫蛍光染色…メサンギウムへのIgA沈着が特徴的
-
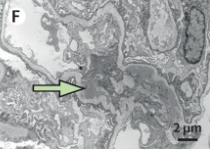
電子顕微鏡…メサンギウムへのelectron-dense depositが特徴的
-
→Oxford分類(MEST-Cスコア)による予後予測が可能
◎治療
-
腎機能正常・24時間蛋白尿<0.75-1.00g→支持療法
-
SGLT2阻害薬が有用…IgA腎症患者の腎不全・死亡リスクを大幅に減少させる(Kidney Int. 2021;100(1):215-224.)
-
-
支持療法3ヵ月実施したが24時間蛋白尿>0.75-1.00g or 腎機能低下進行リスクが高い→ステロイド治療を考慮
- ステロイドの有用性は現状わかっていない
-
メタアナリシス…24時間蛋白尿>1.00gでは有用とされる(Cochrane Database Syst Rev, 3 (2020), Article CD003965)
-
STOP-IgA試験では否定的(欧州、eGFR>60、24時間蛋白尿 1.6±0.8gの患者では有益性なし)(N Engl J Med, 373 (2015), pp. 2225-2236)
-
Testing試験では肯定的(中国人、eGFR>20、 24時間蛋白尿 >1.00gでmPSL6-9ヵ月内服で、腎不全リスク低下)(American Society of Nephrology Kidney Week 2021; November 4–7 (abstr FR-OR61).)
-
- ステロイドの有用性は現状わかっていない
-
その他免疫抑制剤
-
ミコフェノール酸モフェチル(MMF)…良好な結果あり?(Contrib Nephrol, 190 (2017), pp. 108-116)
-
シクロホスファミド(CyC)・アザチオプリン(AZP)…eGFR<60の患者への効果は認められず(J Am Soc Nephrol, 13 (2002), pp. 142-148)
-
リツキシマブ(RTX)…効果不明:効くとする研究もあれば(Arthritis Rheumatol. 2018;70(1):109-114.)、効かないとする研究もある(J Am Soc Nephrol. 2017;28(4):1306-1313.)
-
-
eGFR<30で腎生検上慢性病変進行あり→保存療法。腎代替療法紹介
③ループス腎炎
SLE患者の50-70%に見られる。SLEの予後不良因子の一つ。
◎臨床所見
-
蛋白尿+顕微鏡的血尿、時々白血球尿、高血圧(重度の場合あり)
-
ただし、尿所見は糸球体病変重症度を必ずしも反映しないので注意!
-
増殖性ループス腎炎患者…C3,4低値、抗核抗体陽性、抗dsDNA抗体陽性が多い。抗C1q抗体・抗Sm抗体が見られることもある
-
腎外症状…SLE参照。腎障害をおこす他疾患(シェーグレン症候群、原発性抗リン脂質症候群、混合結合組織病など)との鑑別を。
◎病理
-
ループス腎炎の診断・組織学的傷害パターンの特定に最良の方法
-
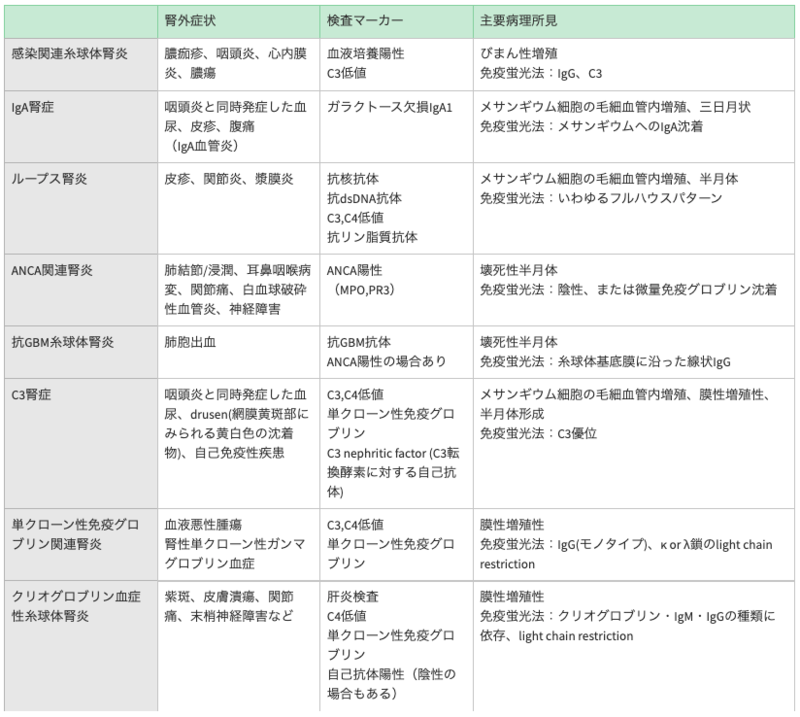
光学顕微鏡…国際腎臓病理学会によるループス腎炎分類を行う→活動性・経過(急性or慢性)を判断
-
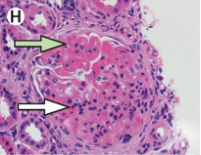
※Ⅲ・Ⅳは、毛細血管内細胞増生、半月体形成、壊死、免疫性微小血栓、ワイヤーループ、毛細血管ループ内の好中球などの病変をおこす
-
ワイヤーループ(緑矢印)、毛細血管内細胞増生(白矢印)
-
-
-
Ⅰ:微小メサンギウムループス腎炎…蛍光抗体法でメサンギウムに免疫沈着物あり。光学顕微鏡は正常。
-
Ⅱ:メサンギウム増殖性ループス腎炎…メサンギウムの増殖のみ
-
Ⅲ:巣状ループス腎炎…病変部が全糸球体の50%未満
-
Ⅳ:びまん性ループス腎炎…病変部が全糸球体の50%以上
-
Ⅴ:膜性ループス腎炎…膜性腎症パターン。Ⅲ,Ⅳと併存する
-
Ⅵ:進行硬化性ループス腎炎…広範な慢性変化で活動性なし。90%以上の糸球体が全節性硬化をおこす。
-
-
Ⅰ,Ⅱ…メサンギウムに沈着
-
Ⅲ,Ⅳ,Ⅴ…毛細血管壁に沿って沈着
-
-
沈着位置はループス腎炎分類によって決まる
-
電子顕微鏡…分類に応じて、メサンギウム・内皮下沈着が見られる
-
Ⅴ…上皮下沈着が見られる
-
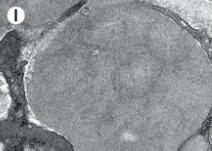
電子密度の高い沈着物は、時に指紋のような部分構造を示す
-
組織学的病変は予後と相関…Ⅲ,Ⅳは予後不良
◎治療
-
classⅠ,Ⅱ…予後良好→免疫抑制剤の必要性は腎外病変と相談
-
lupus podocytopathy→微小変化型病変として管理
- ◎EULAR/KDIGOガイドラインによる寛解導入療法(Ann Rheum Dis. 2020;79(6):713-723.)
1. まずmPSL総量0.5-2.5gを1-3日間静注
2. PSL0.3-1.0mg/kg/dayで後療法
3. 加えてCyC or MMF投与
- CyC…500mg/2w x6回(Euro-Lupus regimen)
- MMF…1-3g/日 x6ヵ月
4. PSLは3-6ヶ月までに7.5mg/day以下に漸減 - 重症例(生検で壊死性半月体形成性糸球体腎炎、腎機能が急速に低下)→より強力な免疫抑制レジメン…ステロイド・MMF・カルシニューリン阻害薬の併用が有用(the National Institutes of Health regimen)(Ann Intern Med. 2015;162(1):18-26.)
-
-
ステロイドパルス(0.5g/day x3日間)
-
4週間経口PSL(0.6mg/kg/日)開始
-
タクロリムス(Tac)2mg x2回/day + MMF0.5g x2回/day
-
PSLは2週間毎に5mg/dayずつ20mg/dayまで漸減→2週間毎に2.5mg/dayずつ10mg/dayまで漸減
-
-
その他新規薬剤
-
voclosporin…低用量PSL+MMFへの併用が有用(AURORA1, Lancet. 2021;397(10289):2070-2080.)
-
Obinutuzumab(抗CD20抗体)、RTXなど
- 参考
-
-
◎モニタリング
-
SLEの免疫学的活性あり(抗dsDNA抗体陽性かつ補体低値)の場合、維持療法継続を推奨
-
臨床データと検査データが一致しない場合(抗dsDNA抗体陽性かつ補体低値だが、蛋白尿・腎機能低下などがある場合)、再度の腎試験を検討
-
末期腎不全の場合、腎移植を検討(移植腎では再発率低い)
-
④ANCA関連糸球体腎炎
-
ANCAは、好中球の顆粒や単球のリソゾーム内のタンパク質に対する抗体である
-
間接免疫蛍光検査では、cytoplasmic ANCA(細胞質ANCA,c-ANCA)とperinuclear ANCA(核周囲ANCA,p-ANCA)に分けれれる
-
c-ANCAはPR3-ANCA、p-ANCAはMPO-ANCAに特異的
◎臨床所見
-
糸球体腎炎はANCA関連血管炎患者の約70%に見られ、MPO-ANCA陽性例・高齢者で多い
◎病理
-
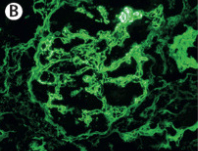
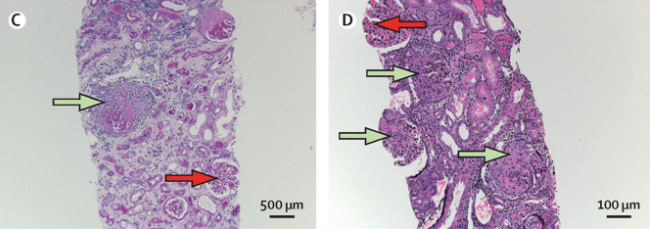
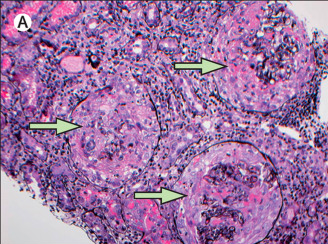
光学顕微鏡…壊死性病変・半月体病変が見られる
-
正常糸球体(赤矢印)と半月体(緑矢印)が混在する(C:MPO-ANCA陽性例、D:PR3-ANCA陽性例)
-
-
免疫蛍光染色…免疫グロブリン・補体の沈着は陰性、あっても微量(pauci-immune)
-
ただし、半月体・壊死部では免疫グロブリン・補体の沈着が軽度見られる場合もある
-
電子顕微鏡…メサンギウム内・毛細血管壁に沿っての少量のsmall electron dense depositが見られる場合もある
◎治療
-
初発・再発例…ステロイド(PSL1mg/kg/day x2週→12週までに20mg/dayまで減量)+CyC or RTXが多い
-
治療の遅れは予後の悪化につながる→腎生検未であっても、診断がついて禁忌(activeな感染症など)が除外され次第、治療を開始するべき
-
CyC…3−6ヵ月内服(POCY)or間欠的静注パルス(IVCY)
-
静脈内投与…①or②で実施
-
①15mg/kgを2週間ごとに3回投与し、その後3週間ごとに3~6ヶ月間投与する。
-
②0.5g/m2 を 2 週に 1 回、3~6 ヵ月投与する。
-
2週間後の白血球数が3500/μL以上、好中球数が1500/μL以上の場合は、次の投与量を0.75g/m2に増量し、再度投与する。
-
-
経口:寛解が得られるまで1日2mg/kgを投与する。白血球数を毎週測定し、投与量を調整する。
-
白血球数は毎週測定し、重度の血球減少を回避するために投与量を調節する。白血球数は3500/μL以上、好中球数は1500/μL以上を維持。最大投与量は200mg/日。
-
-
IVCY年齢別投与量調整:60歳未満では15mg/kg、60-70歳では12.5mg/kg、70歳以上では10mg/kg
-
POCY年齢別投与量調整:60歳未満で2mg/kg/日、60-70歳で1.5mg/kg/日、70歳以上で1.25mg/kg/日
-
腎機能による投与量調整:eGFR 50~75 ml/minの場合は25%、eGFR<50ml/分未満では50%減量
-
-
RTX…非常に有用。IVCY/PSLとの併用に関してはわかっていない部分も多い
-
その他Avacopanも今後PSLの代わりとして使われうる
-
◎モニタリング
-
ただしPR3-ANCA陽性例では難しい→長期免疫抑制療法が望ましい
-
再発は最初の5年間に30~50%で発生する
-
リスク…PR3-ANCA陽性、過去の再発、多発血管炎性肉芽腫症(GPA)の表現型、ANCA力価など
-
B細胞・ANCA力価を指標にRTX投与スケジュール変更が望ましい(MAINRITSAN2, Ann Rheum Dis, 77 (2018), pp. 1143-1149)
-
⑤抗GBM糸球体腎炎
-
Goodpasture症候群…多くの疾患(ANCA関連血管炎が最多)に続発する肺腎症候群を指す
◎臨床所見
-
二峰性の年齢分布を示す…30代・60−70代で多い
-
大半の患者で急速進行性糸球体腎炎を起こし、~60%の患者で肺胞出血を併発する
-
乏尿・無尿の場合もある
-
自己抗体
-
再発率も高く、ANCA関連血管炎同様に維持療法を考慮
◎病理
-
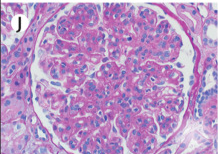
光学顕微鏡…50%以上の糸球体に壊死・半月体形成が見られる
-
-
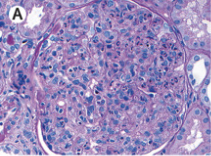
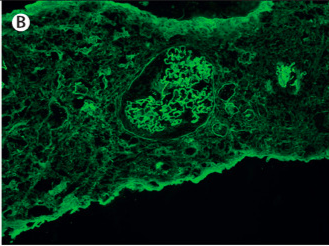
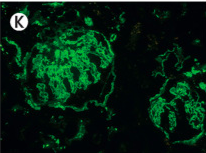
免疫蛍光染色…多クローン性IgG・C3の糸球体基底膜に沿った線状の沈着が特徴的
-
糸球体基底膜に沿った線状のIgG沈着
-
-
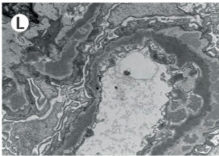
※免疫複合体関連糸球体腎炎では毛細血管壁への沈着、単クローン性免疫グロブリン関連腎症では糸球体基底膜への線状単型沈着
◎治療
-
早期診断・(腎生検前であっても)早期治療が予後を決定する
-
血漿交換…自己抗体の迅速な除去が目的
-
1日1回、2-3週間実施
-
ステロイド…自己抗体の新規形成の予防・抑制が目的
-
RTX…エビデンスは確立していない
-
予後(Ann Intern Med, 134 (2001), pp. 1033-1042)
-
血清Cre<5-7mg/dLは予後良好…1年後腎生存率95%、5年後腎生存率91%
-
血清Cre>5-7mg/dLでも透析を透析不要の場合、1年後腎臓生存率82%、5年後腎生存率50%
-
乏尿、腎生検で円形半月体が高い、透析が必要な腎不全がある場合、他の腎不全原因(急性間質性腎炎など)に続発しない限り、腎機能の回復は期待できない
-
維持療法は基本的には不要
⑥C3腎症
-
補体代替経路の制御異常に伴う補体因子の糸球体沈着によって起こるまれな疾患
-
補体因子の沈着→糸球体の炎症をおこす
◎臨床所見
-
補体は正常の場合あり…C3低値は 47-65%、C4低値は 12-14%のみ(Mayo Clin Proc, 93 (2018), pp. 991-1008)
-
その他、代替補体経路因子の遺伝子変異・自己抗体(C3腎炎因子、抗H因子抗体、抗B因子抗体)が約3分の1で検出される
-
症状進行速度は様々
-
予後予測因子…血清Cre高値、高度蛋白尿(>3g/day)、腎生検で広範な慢性所見
-
感染後糸球体腎炎と推定されたが、血尿/蛋白尿持続・腎機能障害が進行する例では未診断のC3糸球体腎炎である場合がある
◎病理
-
光学顕微鏡…MPGN(膜性増殖性糸球体腎炎)所見が多いが、メサンギウム増殖・半月体形成もありうる
-
膜性増殖性糸球体腎炎パターン
-
-
免疫蛍光染色…免疫グロブリン染色は陰性が多く、C3のみ陽性のことが多い
-
C3染色陽性
-
-
電子顕微鏡…C3糸球体腎炎とdense deposit diseaseの2つに細分化される
-
C3糸球体腎炎…メサンギウム細胞・毛細血管壁への沈着
-
dense deposit disease…ソーセージ状の親水性の高い膜内・メサンギウムへの沈着
◎治療
-
RCTは存在せず、臨床経験・リスク(腎機能障重症度・蛋白尿量・血尿・腎生検所見)を考慮して治療法を決定する
-
軽症(24時間蛋白尿<1-5g。血尿なし)→保存加療
-
中等症以上(蛋白尿量が多いなど)→免疫抑制剤考慮
-
治療薬
-
血尿・24時間蛋白尿>1-5gが持続する患者は再発リスクが高い→無期限での治療推奨
⑦単クローン性免疫グロブリン関連糸球体腎炎
◎臨床所見
◎病理
-
光学顕微鏡…MPGNパターンが多い
-
MIDDの場合、MPGN所見のある結節性硬化糸球体が多い
-
MIDD…糸球体基底膜・尿細管基底膜・メサンギウムへの単クローン性免疫グロブリンの点状沈着
-
免疫蛍光染色…単クローン性免疫グロブリン沈着が多い
-
MIDD…糸球体基底膜・尿細管基底膜への沈着
-
PGNMID…IgG3沈着
-
クリオグロブリン血症…糸球体内腔への沈着
-
イムノタクトイド糸球体症…糸球体の毛細管に沿った沈着
-
電子顕微鏡…様々な所見があり、パターン鑑別に有用
-
MIDD…糸球体基底膜・尿細管基底膜・メサンギウムへの点状沈着
-
PGNMID…メサンギウム・毛細管壁に沿った沈着など
◎治療
-
MIDD…血漿細胞標的療法・自家幹細胞移植で予後大きく改善
-
PGNMID…多くは治療せず、末期腎不全となる。腎移植しても再発率が高い。標準療法はない。
-
原疾患(多発性骨髄腫など)への治療を行うことが多い
-
イムノタクトイド糸球体症…RTXが有用な可能性がある
⑧クリオグロブリン血症性糸球体腎炎
◎臨床所見
-
症状…毛細血管・細動脈への免疫複合体の沈着及びそれに伴う末端臓器障害
-
検査所見
-
C3,4低値(特にC4低値が顕著)