Arthritis Rheumatol. 2022;10.1002/art.42114.
MGHからのANCA関連血管炎(AAV)治療へのエキスパートオピニオンとしてのレビュー
非常に実践的かつ、エキスパートも同じことで悩んでいるんだなということを実感できる内容。
【Keypoint】
-
寛解導入の新薬としてAvacopanが登場し、今後に期待される
-
ANCA検査は診断・フォローにある程度有用だが、病勢そのものの反映というわけではなく注意が必要
-
Covid-19の時代でリスクは増大しているが、Rituximabが寛解導入/維持での第一選択薬である
- 表:活動性AAVへの治療アルゴリズム(エキスパートオピニオン)
- Q1)重症AAVへの最適な寛解導入療法は?
- Q2)ステロイドはどのような量・期間で治療すべきか?
- Q3)ステロイドパルスは必要か?
- Q4)寛解導入の新たな選択肢は?
- Q5)非重症例への治療法は何がよい?
- Q6)治療関連副作用を防ぐため、どのような補助療法を行うべきか?
- Q7)血漿交換の役割は?
- Q8)AAVの再発リスク因子は?
- Q9)診断後、モニターすべき検査は?
- Q10)再発予測因子としてANCA力価は有効か?
- Q11)寛解維持療法として最も有効な方法はなにか?
- Q12)RTXが禁忌/不耐性の場合の寛解維持レジメンは?
- Q13)COVID-19の恐怖は、AAV治療にどのような影響を及ぼすか?
- 【感想】
表:活動性AAVへの治療アルゴリズム(エキスパートオピニオン)
※MTX・MMFは日本では保険適応外
症例)
56歳男性、副鼻腔痛・鼻閉・肺腫瘤影(FigA)で受診
腫瘤の針生検…肉芽腫性炎症、多核巨細胞(FigB)、広範囲の地図状壊死(geographic necrosis)(FigAC
身体所見…多発関節炎、手指チアノーゼ(FigD)、爪線状出血、舌の有痛性潰瘍(FigE)
検査…蛋白尿(2+)、尿中鋳型赤血球、血清Cre1.3mg/dL
血液培養陰性、c-ANCA陽性、PR3-ANCA194U(正常値<20U)
→多発血管炎性肉芽腫症(GPA)と診断。どう治療するか?
Q1)重症AAVへの最適な寛解導入療法は?
-
多数の医師がシクロホスファミド(CyC)を使用し続けている
-
RTX使用不能・RTX投与しても再発する症例にCyCを検討することが最近は多い
Q2)ステロイドはどのような量・期間で治療すべきか?
-
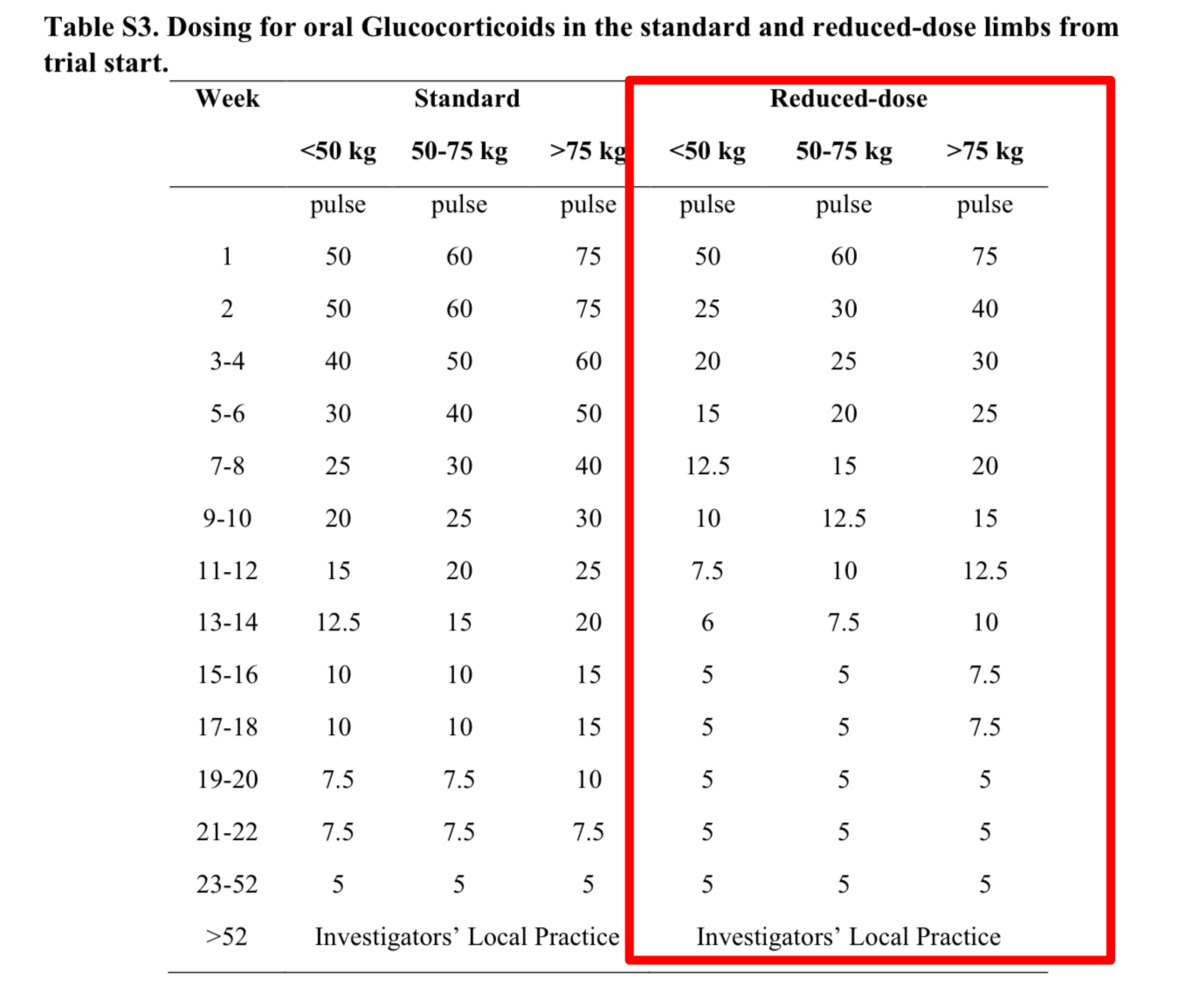
平均的な体格の成人の場合、プレドニゾン(PSL)40-60mg/dayで開始し、4週までに20mg/day、12週までに10mg/day、16週までに5mg/dayに漸減し、5−6ヵ月で中止が望ましい
-
※PEXIVASプロトコル
-
-
ただし、より高用量・長期間の治療が必要な症例もある
Q3)ステロイドパルスは必要か?
-
本当に必要なのかどうかははっきりしない
-
パルスに関しての事後解析では予後に差がないことが示唆されているが、交絡因子の除外が困難
-
重症例の場合、疾患の迅速なコントロール・血管炎の重大合併症を防ぐ目的で、パルスは重要な治療と思われる
-
ただし非重症例の場合、臨床判断でパルスの短縮・投与量の減量・見送りすることが適切である
Q4)寛解導入の新たな選択肢は?
-
Avacopan(C5a受容体拮抗薬)がステロイド・CyC・RTXの補助として有効であることが示されている
-
あくまでもAvacopanは、RTX/CyCとの併用で重症例を効果的に治療する・ステロイド必要量を減らすことを目的として使用すべき
Q5)非重症例への治療法は何がよい?
-
選択肢としてはRTXの他、MTX・MMF・AZAがある
-
「非重症例」の定義…病変が上気道に限局し、急速進行性糸球体腎炎・神経炎・重症炎症性眼疾患・肺胞出血などの重症臓器病変がない
-
ただしMTXは、重症例には効果が低く使用すべきではない
-
ミコフェノール酸モフェチル(MMF)も非重症AAVに有効
-
ただし重症例・再発リスクが高い症例には非推奨
Q6)治療関連副作用を防ぐため、どのような補助療法を行うべきか?
-
明確なデータはないが、患者の臨床像・リスクプロファイルと相談して予防期間を決める
-
エキスパートオピニオン…PSL≦15mg/dayになったらPcP予防中止を検討するが、リンパ球減少が遷延しうる治療(RTX/CyC併用など)を受けている場合はより長期間の予防が適切かもしれない
-
免疫抑制療法によってウイルス感染/再活性化リスクは高くなるが、抗ウイルス薬のルーチン仕様は現状推奨されない
-
肺炎球菌ワクチンについて…13価ワクチン(プレベナー®)をまず接種→少なくとも2ヵ月後に23価ワクチン(ニューモバックス®)を接種すべき
症例続き①)
-
mPSL1g x3日間のステロイドパルスを実施し、その後PSL60mg/day及びCyC150mg経口内服を実施
-
また、ST合剤によるPcP予防を開始
-
劇的に改善し、3日後に退院したが、退院後5日目に血清Cre2.7mg/dLまで上昇、尿検査で蛋白尿・血尿あり、入院
-
RTX1gを2週間隔で計2回実施(CyC無効と判断したわけではなく、RTXを治療の基軸として使用することに決めた)
Q7)血漿交換の役割は?
-
必要性に関しては議論され続けているが、現状ルーチンでの使用は適応外と考えられている
-
ただし、特定の症例には有用性が残っているかもしれない…主要な臓器障害・致死的な疾患活動性のある症例の初期(初期の急速進行性糸球体腎炎・びまん性肺胞出血など)
症例続き②)
-
血漿交換は使用せず治療となった
-
発症から2ヵ月後に透析導入が必要となったが、徐々に腎機能は改善→6週間で透析離脱し、血清Cre1.8mg/dLまで回復した
-
RTX投与から4ヵ月後にサイドのRTX維持投与を行い、5ヵ月後にはプレドニン中止できた
-
治療開始後7ヵ月でANCAは陰転化した
Q8)AAVの再発リスク因子は?
-
AAVの再発は非常に多い
-
再発リスク…PR3-ANCA陽性、GPA、過去の再発歴、ANCA陽性期間が長い(2年以上)、免疫抑制の維持期間が短い(2年以内)
-
MPO-ANCA陽性は高度腎機能障害を起こすことが多いが、再発リスクは低い
Q9)診断後、モニターすべき検査は?
-
疾患活動期は毎週モニター→安定したら検査頻度を減らしていく
-
寛解後、最初の数カ月は毎月、次の2年間は3ヵ月毎、その後4-6ヵ月毎にフォロー
-
ただし、再発を早期発見するため、患者ごとにリスクのある臓器(腎臓など)の検査フォローを考慮
-
ANCA力価を3−6ヵ月毎にフォローし、ANCA陽転化・力価上昇時はモニタリングを綿密に行う
-
ステロイド有害事象チェック…骨密度検査など
-
画像は以下の通り
-
診断時胸部CTをチェックし、治療中も再検して経過観察を行う
-
副鼻腔・眼窩病変→同部位CT
-
髄膜病変→MRI
Q10)再発予測因子としてANCA力価は有効か?
-
AAV管理におけるANCAの価値は3点にまとめられる
症例続き③)
-
ANCAは陰性化したが、数年間に何度か再発を起こした
-
ANCA力価と疾患活動性は緩やかな相関しかなく、再発予測・疾患コントロールとの相関はなかった
-
再発時ステロイド+RTXで治療したが、再発のたびに腎機能は悪化し、最終的に末期腎不全となり腎移植を受けた
-
腎移植から4ヵ月後に両側サイトメガロウイルス網膜炎を発症し、視力障害を起こした
Q11)寛解維持療法として最も有効な方法はなにか?
-
大半の症例で、RTXでの維持療法が推奨される
-
維持療法としてのRTX(6ヵ月毎投与)vs AZAの臨床試験…28ヵ月時点での再発率が優位にRTXで低い(AZA29%、RTX5%)(MAINRITSAN, N Engl J Med 2014;371:1771-80.)
-
ただし維持療法での最適なRTX投与レジメンは現状不明…患者によって適切なレジメンが異なるため
-
大半の症例で維持療法が必要だが、一部症例(軽症MPO-ANCA)では不要な場合がある
-
軽症例では経過観察でOK
-
全症例で永続的なフォローが必要
-
一般的な維持療法は、寛解導入療法後の4-6ヵ月後にRTX投与を行うことである
-
ただし可能ならRTX投与間隔を延長することが、このコロナの時代では可能かつ賢明な選択肢である
-
例…RTX1gの年1回単回投与など
-
頻度は10%未満~50%程度とされる
Q12)RTXが禁忌/不耐性の場合の寛解維持レジメンは?
-
AZA・MTX・MMFが選択肢で、全て妥当
Q13)COVID-19の恐怖は、AAV治療にどのような影響を及ぼすか?
-
RTX等のCD20モノクローナル抗体によるB細胞枯渇によって、Covid-19転機不良・ワクチン反応悪化が起こる
-
RTX使用はTNF阻害薬・MTXと比較してCovid-19重症化・死亡リスクが上昇する(Ann Rheum Dis 2021;80:930-42.)
-
その他、PSL≧10mg/日・疾患活動性が高いといったこともCovid-19重症化リスクである
-
Covid-19への配慮は必要だが、RTXは依然として寛解導入/維持の第一選択薬である
-
以下に留意する
参考
【感想】
-
ANCAフォロー・RTXの使用に関しては、海外のエキスパートでも同じ様に悩んでいることが実感でき、安心した
-
AAVは致死的な疾患だが、適切なタイミング・強度で治療すればある程度寛解・無再発に持っていけるので、治療しがいのある疾患である
-
その分非常に診断・フォローともに難しいのだが…
-
Covid-19がもう少し落ち着き、血管炎についてだけ頭を悩ますことができる時代が待ち望まれるが、厳しいかもしれない…
参考
表:AAV臨床試験一覧
|
試験名
|
寛解導入or維持療法
|
治療レジメン
|
被験者数
|
Primary outcome
|
Primary Result
|
結論
|
|
CYCAZAREM
(N Engl J Med. 2003;349(1):36-44.)
|
維持療法
|
CyC(1.5mg/kg/日)
or
AZA(2mg/kg/day)
|
155
|
18ヵ月での再発率
|
AZA 15.5%
CyC 13.7%(p=0.65)
|
AZAとCyCは、寛解維持において同等の効果
|
|
NORAM
(Arthritis Rheum. 2005;52(8):2461-2469.)
|
寛解導入療法
|
経口CyC(2mg/kg/日)
or
経口MTX(20-25mg/週)
|
100
|
6ヵ月での寛解
|
MTX 89.8%
CyC 93.5%(p=0.041)
|
MTXはCYCに比較して、重症患者・肺病変を有する患者の寛解導入に有効でなかった
|
|
CYCLOPS
(Ann Intern Med. 2009;150(10):670-680.)
|
寛解導入療法
|
静注CyC(15mg/kg/2-3週)
or
CyC(2mg/kg/day)
をPSLと併用
→AZA(2mg/kg/day)へ
|
149
|
寛解までの期間
|
両群で同等
(HR 1.098, 95% CI: 0.78-1.55), p=0.59
|
静注CyCは経口投与と同等の効果があり、白血球減少もなかった
|
|
(JAMA. 2010;304(21):2381-2388.)
|
維持療法
|
CyC+PSLでの寛解導入後
AZA(2mg/kg/日)
vs
MMF(2000mg/日)
|
156
|
無再発期間
|
AZAよりもMMFで再発が多い
(無調整HR1.69)
|
MMFはAZAと比較して、維持療法において劣る
|
|
RAVE
(N Engl J Med. 2010;363(3):221-232.)
|
寛解導入療法
|
RTX(375mg/m^2/週x4回)
vs
CyC(2mg/kg/日)
|
197
|
RTX64%
CyC53%
(p<0.001)
|
RTXはCyCに対して寛解導入において非劣勢
|
|
|
MAINRITSAN
(N Engl J Med. 2014;371(19):1771-1780.)
|
維持療法
|
RTX投与(0,14日目・6,12,18ヵ月)
or
AZA内服(22ヵ月、2mg/kg/日から開始)
|
115
|
28ヵ月での重大な再発
|
再発率
AZA29%
RTX5%
|
AZAはRTXに対して維持療法に老いて劣勢
|
|
MAINRITSAN2
(Ann Rheum Dis. 2018;77(8):1143-1149.)
|
維持療法
|
RTX定期投与(0,14日目・6,12,18ヵ月)
or
個別対応(ベースラインで500mg、CD19+B細胞 or ANCAが再出現したらRTX再投与)
|
162
|
28ヵ月での再発
|
再発率
定期投与9.9%
個別対応17.3%
(p=0.22)
|
再発率は定期投与・個別対応どちらでも同等
個別対応のほうがRTX投与回数が少ない
|
|
EUVAS
(Ann Rheum Dis. 2019;78(3):399-405.)
|
寛解導入療法
|
MMF 2-3g/日
or
静注CyC(15mg/kg、2-3週ごと)→維持はAZAへ
|
140
|
6ヵ月での寛解
ステロイド漸減
|
寛解率
MMF67%
CyC61%
|
|
|
PEXIVAS
(N Engl J Med. 2020;382(7):622-631.)
|
寛解導入療法
|
2x2組入
・血漿交換ありorなし
・ステロイド標準レジメンor減量レジメン
|
352
|
すべての原因での死亡
末期腎不全
|
複合エンドポイント
|
血漿交換は死亡・末期腎不全の発生率を減少させなかった
ステロイド減量レジメンは,標準レジメンに対して非劣性
|
|
ADVOCATE
(N Engl J Med. 2021;384(7):599-609.)
|
寛解導入療法
|
Avacopan30mg2回/日
or
+標準治療(CyC or RTX)
|
331
|
寛解率
Avacopan72.3%
PSL70.1%
(優越性p=0.24)
|
Avacopanは寛解導入において、PSLに対して26週目には非劣勢で、52週目には優れる
|