レビュー本文の方。ざっと要約。
1.概要
GPA:10万人あたり1.3人
MPA:10万人あたり1.6人血管炎全体は42.1人
非重症症状…副鼻腔・鼻腔、粘膜、肺結節、気管支病変、関節炎、強膜炎、壊疽
重症症状…びまん性肺胞出血、糸球体腎炎、ニューロパチー、感覚障害、強皮症
特に重要なのが腎病変で、腎病変を持つ人の30%が5年後には末期腎不全となっている。
2.疫学
-
20%は遺伝的な要因
-
NETsが関与しているものと思われる
3.寛解導入
-
ステロイドは副作用が大きい
-
入れ方は決まったものはないが、パルス療法がよく用いられる。ただエビデンスは弱い。
-
よくあるのは1mg/kg⇨1ヶ月で30-40mgへ⇨3ヶ月で10-20mgへ
-
PEXIVAS studyでは減量ステロイドが非劣性であった
-
減量:標準投与群の55%容量を最初の6ヶ月で使用
-
現在さらなる研究が進行している
-
シクロホスファミド併用
-
PCPリスク⇨バクタ
-
腎機能・年齢に留意して投与量決定
-
経静脈での治療時は、メスな投与し、出血性膀胱炎対策
-
時々採尿して膀胱癌スクリーニング
-
B細胞枯渇等の免疫抑制を起こすアルキル化剤
-
投与によって反応性自体はいいが、再発が多い⇨経口と経静脈を比較する研究が進行している
-
CYCLOPS study:寛解導入でのシクロホスファミドパルスvsシクロホスファミド毎日投与⇨AZAへ…特に違いなし
-
リツキシマブ
-
シクロホスファミドでも寛解導入できなければどうするか?⇨CD20好中球の抑制薬であるリツキシマブ
-
RAVE-trial:197人のGPA/MPAに対して
-
5.5ヶ月のステロイドテーパー+RTX(4週ごと)
-
ステロイド+シクロホスファミド(3-4ヶ月)⇨AZA で比較
-
RTXは4回までで終了(維持はしない)
-
Cre 4.0 mg/dLの腎不全or人工呼吸を必要とするびまん性肺胞出血患者 は除外
-
メインアウトカム:6ヶ月でのステロイドoff率…RTXのほうが良かった(64%vs54%)
-
寛解維持率は非劣性
-
EUVAS-trial・RITUXVAS
-
severe血管炎に対して
-
リツキシマブ+2回経静脈シクロホスファミド
-
3-6ヶ月のシクロホスファミド⇨アザチオプリン
-
寛解率は同レベルで、有害事象も同レベル
-
安全性を考えると、リツキシマブ>シクロホスファミドと思われる(悪性腫瘍がリツキシマブのほうが少ない)
-
ただ、リツキシマブのほうが高いので、シクロホスファミドのほうが選択される場合もある
-
メトトレキサート:細胞外アデノシンを増加させる
-
NORAM-trial
-
非重症GPA/MPA(94%GPA)に対してMTXor毎日CYC
-
MTXは肝障害が多く、CYCは白血球減少が多かった
-
limitation
-
12ヶ月CYC使用したため、6ヶ月時点での比較結果は微妙かもしれない
-
12ヶ月ですべての治療終了としているので、その後のフレアがたくさんあった
-
MTXは使い慣れた薬なのでいい選択肢。ただ、腎機能低下症例には使えない
-
ミコフェノール酸モフェチル:DNA合成の阻害
-
MYCYC-trial…MMFvsCYC
-
非重症の血管炎に対して
-
MMF(ミコフェノール酸2 g /日 76%)
-
シクロホスファミドパルス を比較
-
重症・急性腎障害は除外されたが、81%に腎障害があり、NORAMと比較して腎障害の重症度は高い
-
⇨重症度低いなら考慮
-
血漿交換
-
有用性は揺らいでいる。
-
MEPEX-trial
-
Cre>5.8 mg/dLかつ生検で糸球体腎炎が証明されたAAV患者における血漿交換の有効性を評価する唯一の大規模試験
-
経口シクロホスファミドおよび7回の血漿交換 と 3日間のパルス⇨グルココルチコイドテーパー を比較
-
血漿交換群のほうが、生存率・透析非導入・3ヶ月後のCre<5.8群が多かった
-
ただ、その4年後の追跡調査では生存率・末期腎不全率は有意差なかった。
-
PEXIVAS
-
腎炎/肺胞出血のあるAAV患者に対して
-
標準治療のみ で比較
-
7年時点で死亡率・末期腎不全率は変化なし
-
⇨双方合わせるとあまり血漿交換には意味ないかもしれない
-
寛解導入まとめ
4.寛解維持
-
長期間免疫抑制をするということ、血管炎の再発率を天秤にかけて寛解維持を行う必要あり。
-
血管炎の診断から1年以上経過して発生する死亡例の大半が感染が原因である。
-
内服薬
-
候補はシクロホスファミド・アザチオプリン・メトトレキサート・ミコフェノール酸モフェチル
-
CYCAZERAM
-
アザチオプリンvsシクロホスファミド
-
18ヶ月時点での再発率は同様(15.5% v 13.7%; P=0.65)
-
⇨シクロホスファミド投与は3-6ヶ月に限定させる方向となった
-
WEGENT
-
メトトレキサートvsアザチオプリン
-
有害事象は有意差なし (メトトレキサートvsアザチオプリン 19% v 11%; P=0.21)
-
メトトレキサートで有害事象が多かったのは腎機能に合わせての容量調整がなかったためかもしれない
-
生存率も差はなかったが、評価困難
-
アザチオプリンvsミコフェノール酸モフェチル
-
再発率は、アザチオプリンがミコフェノール酸モフェチルより低かった
-
ミコフェノール酸モフェチルも大対訳として使えるかもしれない。ただ、MYCYCでは有効性あったが、アザチオプリンには劣る。特にGPA・PR3-ANCA陽性例ではイマイチで重症化している。
-
リツキシマブ
-
寛解導入で重要な薬だが、維持での使用に関してもRCTがある。
-
MAINRITSAN1
-
新規/再発症例に対するリツキシマブvsアザチオプリン
-
リツキシマブ:500 mg 2週で2回⇨18ヶ月まで半年ごとに投与
-
アザチオプリン:22ヶ月
-
アザチオプリンのほうが重度の再発率は高かった (29% v 5%; hazard ratio 6.61, 1.56 to 27.96)
-
リツキシマブ最終投与から42ヵ月後の5年後の時点で、リツキシマブはアザチオプリンよりも優れていたが、両群とも無再発生存率は低下した(58%対37%;P=0.01)
-
5年後生存率もリツキシマブのほうが高い
-
費用対効果も良いようである
-
RITAZAREM study
-
再発症例に対するリツキシマブvsアザチオプリン
-
リツキシマブ:1g・4ヶ月おき
-
再発率はリツキシマブで低かった (13% v 38%; hazard ratio 0.30, 0.15 to 0.60; P<0.001)
-
さらなる研究が求められる
-
リツキシマブのタイミング
-
MAINRITSAN2
-
末梢B細胞が検知されない・ANCA力価が高い、という条件はフレアを予測する因子である。
-
固定間隔アプローチとテーラメイドアプローチは、再発リスク同等
-
28ヶ月間の重症/非重症再発はテーラーメイドアプローチで有意に少なかった
-
テーラメイドアプローチのほうがリツキシマブ投与は少なく、安全性は同等(85% v 91% severe events; P=0.5)
-
まだリツキシマブのタイミング・容量は不確定だが、個別化治療になっていくものと思われる。
-
治療期間
-
よく分かっていない
-
無投薬寛解を維持できる人もいるが、再発は時間経過とともに増えていく
-
REMAIN-trial
-
アザチオプリンとプレドニゾンを24ヵ月後に中止 vs48ヵ月間治療を継続
-
中止群で、非重症/重症の再発リスク・末期腎不全率が高い
-
メタ解析:プレドニンによる長期治療は、短期間治療と比較して再発が少ない
-
再発リスクに応じて患者を分類することで、個別化治療が可能になっていくものと思われる
-
重度腎障害と再発リスク低下は相関している
-
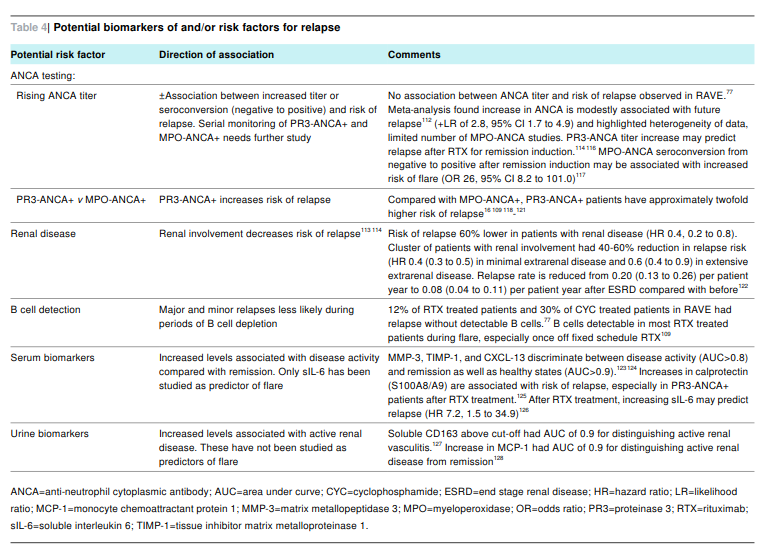
再発を予測するバイオマーカーの研究が進んでいる
-
ANCA力価上昇、ANCA陰性例の陽性化
-
PR3-ANCA陽性…MPO-ANCA陽性例より高リスク
-
腎病変
-
B細胞検出
-
血清マーカー…sIL-6
-
尿に関しては研究中
-
臓器特異的な治療…副鼻腔・気管支・眼窩偽腫瘍・間質性肺疾患
-
エビデンスはあまりない
-
副鼻腔
-
診断は耳鼻科専門医にやってもらうと良いかもしれない。
-
特徴的な所見は鞍鼻・鼻中隔穿孔
-
骨びらん、持続的な鼻づまり、痂皮化、鼻出血が治療後も継続する可能性あり
-
特異的な治療はない。
-
気管支病変
-
喉頭蓋下狭窄、気管支炎、気管支瘤があるが、かなりまれ
-
免疫抑制療法しても起こりうる(気管支は疾患活動性との相関が乏しい)
-
気管支腫瘤の治療
-
気管内グルココルチコイドと拡張術
-
全身免疫抑制
-
眼窩炎症
-
治療への反応性が乏しく、再発することが多い
-
間質性肺疾患
-
MPOーANCAと関連あり
-
治療法はよく分かっていないが、免疫抑制が多い。
-
抗線維化薬(ニンテダニブ)が有望視されている
-
補完治療
-
ST合剤:PCP予防
-
特にRCTはないが、PSL20mg以上・4週間以上内服する患者(特に他の免疫抑制薬を併用する場合)は予防内服するようアメリカ胸部学会から勧告が出ている
-
AAV再発を減らすという役割があるともされるが、よく分かっていない
-
臓器移植
-
腎移植は安全で、透析よりも勧められる
-
腎移植前の12ヶ月でANCA力価陰性を保つ必要あり
-
肺移植に関してはよくわかっていない
-
うつ・不安の合併率が一般人口よりも高い
-
⇨心理的介入も重要である
-
新規治療
-
C5aを標的としたモノクローナル抗体
-
細胞傷害性Tリンパ球治療薬アバタセプト